Oxid uhličitý (CO2)
Oxid uhličitý (CO2)
- Základní informace
- Ohlašovací prahy pro úniky a přenosy pro ohlašování do IRZ/E-PRTR
- Základní charakteristika
- Použití
- Zdroje úniků
- Dopady na životní prostředí
- Dopady na zdraví člověka, rizika
- Celkové zhodnocení nebezpečnosti z hlediska životního prostředí
- Způsoby zjišťování a měření
- Další informace, zajímavosti
- Informační zdroje
Základní informace
| Pořadové číslo látky v IRZ/E-PRTR | 3 |
| Další názvy | suchý led, obsažen v kyselině uhličité |
| Číslo CAS | 124-38-9 |
| Chemický vzorec | CO2 |
Ohlašovací prahy pro úniky a přenosy pro ohlašování do IRZ/E-PRTR
| Úniky do ovzduší (kg/rok) | 100 000 000 |
| Úniky do vody (kg/rok) | - |
| Úniky do půdy (kg/rok) | - |
| Přenosy v odpadních vodách (kg/rok) | - |
| Přenosy v odpadech (kg/rok) | - |
| Rizikové složky životního prostředí | ovzduší |
Základní charakteristika
Oxid uhličitý je bezbarvý plyn bez zápachu. Při nadýchání ve větším množství působí štiplavě na sliznicích a vytváří kyselou chuť. To je způsobeno jeho rozpouštěním na vlhkých sliznicích a ve slinách za vzniku slabého roztoku kyseliny uhličité. Při ochlazení na -78 °C oxid uhličitý přechází do tuhého skupenství a vzniká bílá tuhá látka, tzv. suchý led. Kapalný může existovat jen za tlaku vyššího než přibližně 500 kPa (~5-ti násobek atmosférického tlaku). Jedná se o látku nepříliš reaktivní a nehořlavou. Je konečným stupněm oxidace uhlíku (organických látek) a výsledkem hoření za dostatečného přístupu kyslíku. Hustotou 1,98 kg.m-3 je plynný oxid uhličitý zhruba 1,5 x těžší než vzduch.
Použití
Stlačený nebo tuhý oxid uhličitý je využíván v potravinářském průmyslu a jako chladivo zejména při přepravě mražených výrobků. Dále je využíván pro výrobu šumivých nápojů a sodové vody. Oxid uhličitý je některými výrobci přidáván do piva a šumivých vín, přestože je zde obsažen díky přirozeným fermentačním pochodům. Další oblastí použití je kypření těst, kterého se dosahuje buď využitím kvasnic vytvářejících oxid uhličitý biologicky, nebo kypřícími přísadami, které oxid uhličitý uvolňují buď zahřátím, nebo působením kyseliny. Rovněž je využíván jako ochranná atmosféra.
Oxid uhličitý je rovněž používán jako levný a nehořlavý stlačený plyn pro nafukování záchranných vest či člunů. Malé bombičky slouží jako zdroj hnacího plynu pro vzduchové pušky či zbraně na paintball i k domácí výrobě sifonu.
Nehořlavost oxidu uhličitého je využívána v podobě hasicích přístrojů plněných kapalným oxidem uhličitým. Z důvodu své velmi nízké ceny se využívá i jako ochranná atmosféra pro svařování kovů, přestože sváry vytvořené v ochranné atmosféře vzácných plynů helia či argonu jsou prokazatelně kvalitnější.
Kapalný oxid uhličitý je dobré rozpouštědlo pro řadu organických látek a je využíván například k extrakci kofeinu z kávy. Začal rovněž přitahovat pozornost farmaceutického i chemického průmyslu jako méně toxická alternativa pro tradičně používaná rozpouštědla na bázi chlorovaných organických látek.
Oxid uhličitý je někdy přidáván na omezenou dobu (několik hodin) do atmosféry skleníků s cílem podpořit růst rostlin a především vyhubit škůdce jako moly, svilušky a další, jimž zvýšená koncentrace oxidu uhličitého v ovzduší škodí.
Suchý led (tuhý oxid uhličitý) je využíván v divadlech a při hudebních představeních ke tvorbě zvláštních efektů. Po vložení do vody suchý led sublimuje a vznikající směs oxidu uhličitého a kondenzované vodní páry vytváří efekt mlhy těžší než vzduch.
Další uplatnění lze nalézt v medicíně (stabilizace rovnováhy kyslík/oxid uhličitý v krvi) a v průmyslových laserech. Může být rovněž využit při těžbě ropy, kdy je injektován buď přímo do vrtu nebo do jeho blízkého okolí, kde jednak působí zvýšení tlaku a jednak se v surové ropě rozpouští a snižuje tak její viskozitu.
Zdroje úniků
Přirozeným zdrojem emisí oxidu uhličitého je dýchání aerobních organismů, zatímco procesem vedoucím k jeho přirozenému úbytku je fotosyntéza zelených rostlin a absorpce oceány. Tyto přírodní pochody působí protichůdně a výsledkem by byl v podstatě vyvážený stav. Mezi další přírodní pochody emitující oxid uhličitý patří požáry a vulkanická činnost.
Do koncentrace oxidu uhličitého v atmosféře zásadním způsobem promlouvá člověk, konkrétně spalování fosilních uhlíkatých paliv, které představuje velmi významný zdroj emisí. Ostatní antropogenní emise ve srovnání se spalováním zaslouží označení jako málo důležité. Oxid uhličitý je emitován všude tam, kde dochází ke spalovacím procesům uhlíkatých fosilních paliv – zemního plynu, ropných produktů, uhlí, koksu. Uvádí se, že energetickým využíváním 1 tuny odpadů se zamezí emisi zhruba 1 tuny ekvivalentu CO2. Zdrojem emisí je samozřejmě i spalování paliv biologického původu – biomasy, dřeva, bionafty a bioplynu. Podíl dopravy na tvorbě CO2 se odhaduje na 10 – 15 %. Emise oxidu uhličitého u vozidel se spalovacími motory jsou bezprostředně určeny spotřebou paliva.
Zdrojem emisí oxidu uhličitého jsou průmyslové provozy, kde se buď využívá spalování či termických procesů, nebo je surovinou například vápenec a dochází k emisím oxidu uhličitého:
- Spalovací procesy (uhlíkatá paliva);
- Koksárenství;
- Rafinerie olejů a plynu;
- Hutnictví a kovoprůmysl;
- Cementárny;
- Sklárny, výroba keramiky;
- Tavení nerostných materiálů;
- Zpracování celulózy a dřeva;
- Předúprava vláken a textilií, vydělávání kůží a kožešin;
- Zařízení na zneškodňování uhynulých zvířat.
Protože oxid uhličitý jako takový nachází použití v celé řadě odvětví a je využíván k nejrůznějším účelům, existuje rovněž široká možnost jeho emisí do atmosféry. Shrneme-li oblasti, kde se oxid uhličitý přímo využívá a může tudíž unikat do životního prostředí, vychází následující výčet:
- Potravinářský průmysl;
- Využití v podobě stlačeného plynu;
- Hašení hasicími přístroji s náplní kapalného oxidu uhličitého;
- Svařování v ochranné atmosféře oxidu uhličitého;
- Farmaceutický a chemický průmysl (alternativní rozpouštědlo);
- Zemědělská činnost (úprava složení atmosfér skleníků).
Dopady na životní prostředí
Oxid uhličitý v atmosféře absorbuje infračervené záření zemského povrchu, které by jinak uniklo do vesmírného prostoru, a přispívá tak ke vzniku tzv. skleníkového efektu a následně ke globálnímu oteplování planety. Někdy je oxid uhličitý označován jako jediná příčina vzniku skleníkového efektu, to však není přesné, protože k jeho vzniku přispívají i jiné látky. Oxid uhličitý však ve vzniku skleníkového efektu hraje hlavní roli. Koncentrace oxidu uhličitého v atmosféře se neustále zvyšuje.
Dopady na zdraví člověka, rizika
Oxid uhličitý není toxický v pravém slova smyslu ale je nedýchatelný. Dráždivý účinek je při inhalaci zanedbatelný, hlavní účinek je stimulace dýchání (prohloubení a zrychlení dechu) vedoucí až k ochrnutí dýchání. Koncentrace oxidu uhličitého v atmosféře je však velice nízká a nepředstavuje proto pro zdraví přímé riziko.
Ve vyšších koncentracích (například v nedostatečně větraných prostorách) však toxické působení vykazovat může. Krátkodobá expozice oxidu uhličitému může ihned nebo jen s krátkou časovou prodlevou způsobit bolest hlavy, závratě, dýchací potíže, třes, zmatenost a zvonění v uších. Vyšší expozice pak může způsobit křeče, kóma a smrt. Některé vážnější případy otrav mohou zanechat následky na mozku, způsobit změny osobnosti a poškození zraku. Nebezpečí hrozí například v silážních či kanalizačních prostorech.
V České republice platí pro koncentrace oxidu uhličitého následující limity v ovzduší pracovišť: PEL – 9 000 mg.m-3, NPK - P - 45 000 mg.m-3.
Rizikem při nakládání se suchým ledem nebo kapalným oxidem uhličitým jsou v případě přímého kontaktu omrzliny (místní poškození tkáně při teplotě nad -78 °C).
Celkové zhodnocení nebezpečnosti z hlediska životního prostředí
Oxid uhličitý je hlavním plynem přispívajícím k intenzifikaci skleníkového efektu a následně k oteplování planety. Nelze ho sice považovat za přímo nebezpečnou jedovatou látku (vyjma přímého nadýchání), avšak jeho dopady na globální klima jsou skrze skleníkový efekt velmi závažné. Světová meteorologická stanice varuje, že koncentrace skleníkových plynů za rok 2018 dosáhlo nového maxima (408 ppm CO2). Problémem je nejen zvyšování teploty Země ale také rozpouštění CO2 v moři (s rostoucí koncentrací CO2 ve vzduchu, jímají přebytky oceány) a tím se voda okyseluje (vzniká kyselina uhličitá) a to způsobuje největší problémy korýšům s vápníkovou schránkou a také korálům a to má zásadní vliv na potravní řetězce a následné porušování rovnováhy i v oceánech.
Způsoby zjišťování a měření
Z daleka největším zdrojem emisí jsou spalovací procesy uhlíkatých paliv. Ohlašovací práh 100 000 000 kg, tedy 100 000 tun ročně, je tak velké množství, že pravděpodobně nebude mnoho jiných procesů než spalování, u kterých by mohl být práh překročen.
K odhadu produkce oxidu uhličitého spalováním lze použít jednoduchý bilanční výpočet ze známého spotřebovaného množství paliva. Jako krajní možnost můžeme zvolit palivo zemní plyn (methan, nejmenší poměr C:H) a koks (prakticky čistý uhlík). Z bilančního výpočtu plyne, že úplným spálením 1 kg methanu (přibližně 2 m3 za tlaku 101,325 kPa a teploty 20°C), resp. 1 kg koksu vznikne 2,74 kg, resp. 3,66 kg oxidu uhličitého. Zejména případ koksu je velice důležitý, protože se jedná o maximální množství oxidu uhličitého, které může z jakéhokoli uhlíkatého paliva vzniknout. Jiné složení paliva (např. uhlovodíky), obsah popelovin a dalších příměsí tento poměr jen snižují. Pro bezpečně nadhodnocený odhad produkce oxidu uhličitého proto postačuje vynásobit hmotnost spotřebovaného paliva 3,66. Odhad lze zpřesnit výpočtem ze složení konkrétního paliva, kdy je cílem vypočítat, kolik obsahuje 1 kg paliva uhlíku. Poté stačí opět tuto hmotnost vynásobit 3,66 a získáváme hmotnost oxidu uhličitého.
Tam, kde je surovinou vápenec, může jako vodítko posloužit příklad: z 1 kg čistého vápence (CaCO3) vznikne například pražením či jinou reakcí přibližně 0,44 kg oxidu uhličitého (v případě teoretického 100% výtěžku).
Obsah oxidu uhličitého ve spalinách či emitovaných vzdušinách lze přímo měřit s využitím mobilních přístrojů založených na infračervené spektrometrii, případně na refraktometrii. Další možností jsou termické analyzátory a metody spektrofotometrie a nefelometrie. Měření mohou zajistit komerční laboratoře. Produkce oxidu uhličitého je potom součinem jeho koncentrace a objemu vypuštěného plynu.
Pro stanovení CO2 je k dispozici normovaný postup:
| Norma | Metoda měření | Oblast použití |
| ISO 12039:2001 | Stanovení CO2, CO a O2 – výkonové charakteristiky a kalibrace automatizovaných měřicích systémů | Kvalita ovzduší, emise ze stacionárních zdrojů |
Další informace, zajímavosti
Navzdory tomu, že jeho koncentrace v atmosféře je velice nízká, je oxid uhličitý velice důležitou složkou, protože přispívá k intenzifikaci skleníkového efektu a oteplování planety. Na tomto místě je vhodné zdůraznit, že přítomnost oxidu uhličitého v atmosféře je pro život nezbytná – jednak představuje zdroj uhlíku pro zelené rostliny (fotosyntéza) a jednak udržuje díky skleníkovému efektu stabilní a příznivé atmosférické podmínky pro život. V počátcích vývoje Země byl oxid uhličitý emitovaný vulkanicky nezbytnou podmínkou pro vývoj příznivého klimatu na Zemi, což vůbec umožnilo vznik a vývoj života. Současný problém spočívá v tom, že např. spalování fosilních paliv člověkem emituje do atmosféry ohromné množství oxidu uhličitého, množství větší, než jsou schopny přirozené pochody zpětně odstranit. Proto koncentrace oxidu uhličitého v atmosféře od průmyslové revoluce neustále stoupá. V roce 2004 obsahovala atmosféra planety Země 0,038 % obj. oxidu uhličitého, což představuje hmotnost 2,7.1012 tun. Pro dokreslení objemu dopadů lidské činnosti na životní prostředí může sloužit tento příklad - vulkanická aktivita v současné době emituje do atmosféry přibližně 200 mil. tun oxidu uhličitého ročně, což je však jen asi 1 % ve srovnání s emisemi způsobenými lidskou činností (hlavně spalováním fosilních paliv uložených pod povrchem obsahujících obrovské množství uhlíku, který se však před jeho spálením neúčastnil globálního uhlíkového cyklu). Za posledních 50 let se průměrná koncentrace oxidu uhličitého v atmosféře zvýšila z hodnoty 0,0316 % obj. na uvedenou hodnotu 0,0380 % obj. v roce 2004. Nárůst naměřené koncentrace je znázorněn na obrázku 1.
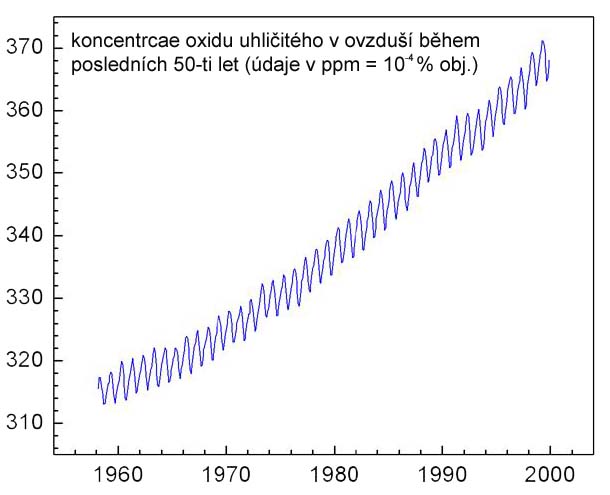
Obrázek 1: Vývoj koncentrace oxidu uhličitého v ovzduší
Prudký nárůst emisí oxidu uhličitého s rozdělením podle jeho původu během posledních 200 let je evidentní z obrázku 2.

Obrázek 2: Emise oxidu uhličitého podle původu
Do vývoje obsahu oxidu uhličitého v atmosféře nepříznivě promlouvá i mýcení deštných pralesů, které mají obrovskou schopnost absorbovat oxid uhličitý z atmosféry fotosyntézou. Právě fotosyntéza zelených rostlin, při které se působením slunečního záření tvoří z "jednoduchého" oxidu uhličitého a vody složité organické látky, je hlavním přirozeným procesem spotřebovávajícím oxid uhličitý z atmosféry. Dalším takovým procesem je jeho absorpce v oceánech, kde je poté zabudováván do vápenatých schránek živočichů (například korálů).
Existují návrhy projektů, které berou uvedené skutečnosti vážně v úvahu a navrhují například systém, ve kterém cílené probublávání speciálních nádrží spalinami (tzn. oxidem uhličitým) podporuje intenzivní růst řas (tím je odstraňován oxid uhličitý), ze kterých by byla následně vyráběna bionafta. Spalování paliv biologického původu, zejména biomasy a bionafty, by potom z hlediska emisí oxidu uhličitého bylo vyváženo tím, že k jejich vzniku by byl nejprve oxid uhličitý z atmosféry spotřebován a fotosyntézou přeměněn na spalovanou biomasu, což v podstatě kopíruje uzavřený přírodní cyklus.
Od roku 2014 mapuje výskyt oxidu uhličitého družice NASA. Situace je natolik závažná, že musí dojít k řadě opatření. V Madridu se konala 2. – 13. prosince Konference OSN o změnách klimatu (COP25), jejímž tématem byly způsoby uplatňování pařížské klimatické dohody z roku 2015 a obecně boj proti globálnímu oteplování. Součástí dokumentu pařížské dohody jsou závazky jednotlivých zemí omezit emise skleníkových plynů, které mají státy od roku 2015 každých pět let aktualizovat. Madridská klimatická konference tak zahájila klíčové období trvající do konce roku 2020, během kterého musí zhruba 200 signatářů dohody představit nové národní klimatické cíle. Program OSN pro životní prostředí vydal zprávu, v níž varuje, že pokud by se země držely svých stávajících slibů ohledně snižování emisí, stouply by teploty do konce století o 3,2 stupně, což by mělo pro klima ničivé důsledky.
Informační zdroje
- Encyklopedie Wikipedia, https://cs.wikipedia.org/wiki/Oxid_uhli%C4%8Dit%C3%BD, https://en.wikipedia.org/wiki/Carbon_dioxide
- Agency for Toxic Substances and Disease Registry, https://www.atsdr.cdc.gov
- Environment Agency, https://www.gov.uk/government/organisations/environment-agency
- Scorecard, The Pollution Information Site, http://scorecard.goodguide.com/chemical-profiles/summary.tcl?edf_substance_id=+124-38-9
- PubChem, Open Chemistry Database, https://pubchem.ncbi.nlm.nih.gov/compound/280
- Centers for Disease Control and Prevention, https://www.cdc.gov/niosh/idlh/124389.html
- US EPA IRIS, https://www.epa.gov/emc/performance-specification-3-oxygen-and-carbon-dioxide
- Milan Popl, Jan Fähnrich: Analytická chemie životního prostředí, VŠCHT Praha, 1999
- Ivan Víden: Chemie ovzduší, VŠCHT Praha, 2005
- VanLoon G.W., Duffy S.J.: Environmental Chemistry a Global Perspective, Oxford University Press, 2005
- Vejvoda J., Machač P., Buryan P.: Technologie ochrany ovzduší a čištění odpadních plynů, VŠCHT Praha, 2002
- Linhart J: Toxikologie, VŠCHT Praha, 2014
- Kuraš M.: Odpady a jejich zpracování, Ekomonitor spol. s r.o., ISBN 978-80-86832-80-7
- Encyklopedie Britannica, https://www.britannica.com/science/carbon-dioxide
- European Industrial Emissions Portal, https://industry.eea.europa.eu/pollutants/pollutant-index
- ČSN online, https://csnonline.agentura-cas.cz/
- Right to Know Hazardous Substance Fact Sheets, State of New Jersey Department of Health, https://web.doh.state.nj.us/rtkhsfs/indexfs.aspx