Kadmium a sloučeniny (jako Cd)
Kadmium a sloučeniny (jako Cd)
- Základní informace
- Ohlašovací prahy pro úniky a přenosy pro ohlašování do IRZ/E-PRTR
- H- a P-věty
- Základní charakteristika
- Použití
- Zdroje úniků
- Dopady na životní prostředí
- Dopady na zdraví člověka, rizika
- Celkové zhodnocení nebezpečnosti z hlediska životního prostředí
- Způsoby zjišťování a měření
- Další informace, zajímavosti
- Informační zdroje
Základní informace
| Pořadové číslo látky v IRZ/E-PRTR | 18 |
| Další názvy | - |
| Číslo CAS | 7440-43-9 |
| Chemický vzorec | Cd |
Ohlašovací prahy pro úniky a přenosy pro ohlašování do IRZ/E-PRTR
| Úniky do ovzduší (kg/rok) | 10 |
| Úniky do vody (kg/rok) | 5 |
| Úniky do půdy (kg/rok) | 5 |
| Přenosy v odpadních vodách (kg/rok) | 5 |
| Přenosy v odpadech (kg/rok) | 5 |
| Rizikové složky životního prostředí | ovzduší, voda, půda |
H- a P-věty
| Číslo CAS 7440-43-9; Indexové číslo 048-002-00-0* | |
| Standardní věty o nebezpečnosti | Pokyny pro bezpečné zacházení |
H330 Při vdechování může způsobit smrt H341 Podezření na genetické poškození H350 Může vyvolat rakovinu H361fd Podezření na poškození reprodukční schopnosti nebo plodu v těle matky H372 Způsobuje poškození orgánů při prodloužené nebo opakované expozici H400 Vysoce toxický pro vodní organismy H410 Vysoce toxický pro vodní organismy, s dlouhodobými účinky | P260 Nevdechujte prach/dým/plyn/mlhu/páry/ aerosoly. P271 Používejte pouze venku nebo v dobře větraných prostorách. P284 V případě nedostatečného větrání používejte vybavení pro ochranu dýchacích cest. P304+P340 Při vdechnutí: Přeneste osobu na čerstvý vzduch a ponechte ji v poloze usnadňující dýchání. P310 Okamžitě volejte Toxikologické informační středisko/lékaře/… P201 Před použitím si obstarejte speciální instrukce. P202 Nepoužívejte, dokud jste si nepřečetli všechny bezpečnostní pokyny a neporozuměli jim. P280 Používejte ochranné rukavice/ochranný oděv/ochranné brýle/obličejový štít. P308+P313 Při expozici nebo podezření na ni: Vyhledejte lékařskou pomoc/ošetření. P270 Při používání tohoto výrobku nejezte, nepijte ani nekuřte. P314 Necítíte-li se dobře, vyhledejte lékařskou pomoc/ošetření. P273 Zabraňte uvolnění do životního prostředí. P391 Uniklý produkt seberte. |
* Indexové číslo, harmonizovaná klasifikace dle přílohy VI, nařízení (ES) č. 1272/2008, ve znění pozdějších předpisů.
Základní charakteristika
Kadmium patří mezi těžké kovy, je stříbřitý, měkký, kujný a tažný kov s nízkou teplotou tání (767 °C). Svými vlastnostmi se podobá zinku. Kadmiové prachy obsahují různé sloučeniny kadmia, například chlorid kademnatý. Dýmy kadmia se skládají z malých částeček kadmia nebo oxidu kademnatého (vzniká během spalování). Nejběžnějším oxidačním stavem je +2, může se ale vyskytovat i v oxidačním stavu +1.
Použití
Vzhledem k prokázané toxicitě kadmia se v poslední době projevuje snaha o co největší omezení jeho využívání. EU nařizuje směrnicí RoHS (Restriction of the use of certain hazardous substances in electrical and electronic equipment) od 1. července 2006 povinnost zajistit, aby nová elektrická a elektonická zařízení neobsahovala kadmium a jiné nebezpečné látky (Pb, Cr6+, Hg, zpomalovače hoření - polybromované bifenyly, polybromovaný difenylether). Omezení se netýká průmyslových, telekomunikačních, zdravotnických, vědeckých zařízení s dlouhou životností, která se vyrábějí v malých množstvích. Největší množství kadmia slouží k výrobě baterií, hlavně Ni-Cd a solárních baterií Uplatnění nalézá stále při výrobě lehkotavitelných slitin, pájecích kovů, polovodičů, speciálních kovových slitinách (letectví, jaderná energetika) i v laboratorních přístrojích. Kadmium se používalo na výrobu pigmentů (červený a žlutý pigment barev), jako stabilizátory plastů (PVC), k legování mědi a pokovování. V minulosti se Cd používalo i při výrobě domácích spotřebičů jako jsou vysavače, chladničky, myčky, televizní a rozhlasové přijímače. Kovové kadmium se v menší míře využívá v jaderné technice k absorpci neutronů. Některé sloučeniny kadmia slouží jako fungicidy.
Zdroje úniků
Kadmium se v přírodě vyskytuje vzácně. Mezi chemickými prvky zemské kůry je na 67. místě. Cd doprovází zinečnaté rudy. Z přirozených zdrojů kadmia jsou nejvýznamnější sopečné výbuchy. Emise kadmia do ovzduší způsobené člověkem jsou přibližně 8x vyšší než emise přirozené.
Do ovzduší se kadmium dostává při jeho těžbě, výrobě a zpracování. Významným zdrojem je také spalování fosilních paliv a komunálního a nemocničního odpadu. Zdrojem emisí kadmia do vod jsou odpadní vody z galvanického pokovování a z výroby Ni-Cd baterií. Dalším zdrojem je atmosférická depozice a splach z půd. Nejvýznamnějším přírodním zdrojem kadmia jsou výbuchy podmořských sopek.
Kadmium se v malém množství vyskytuje v půdě a horninovém prostředí. Do půdy se dostává hlavně atmosférickou depozicí městských průmyslových aerosolů, hnojením fosfátovými hnojivy kontaminovanými kadmiem a zavážením čistírenských kalů na pole. Lokálním zdrojem mohou být tekuté a pevné odpady zvířat a lidí, dále také odpady po těžbě a průmyslové (galvanovny) a zemědělské činnosti.
Mezi hlavní antropogenní emise kadmia patří:
- Těžba a zpracování kadmia;
- Spalování fosilních paliv a odpadů;
- Hnojení fosfátovými hnojivy s obsahem kadmia;
- Využití čistírenských kalů (spalování, aplikace na půdy);
- Galvanické pokovování a výroba Ni-Cd akumulátorů.
Dopady na životní prostředí
Kadmium se může vázat na popílek, prachové a půdní částice a jílové půdy. Vazba je nejsilnější u popílku a jílových částic. Kadmium uvolňované do atmosféry se proto váže na emitované částice popílku. Tyto částice mohou zůstat v atmosféře více než týden, než pomocí atmosférické depozice přejdou do vody nebo půdy. Tímto způsobem se kadmium může distribuovat na velké vzdálenosti.
Na zemi se kadmium naváže na částice jílu nebo prachu. V této podobě se může dešťovou vodou vymýt do vodního prostředí nebo může být akumulováno organismy. Akumulace organismy je velmi vysoká, proto dochází ke hromadění kadmia v potravních řetězcích. Popsanou vlastnost lze nazývat bioakumulací. Vysoké koncentrace kadmia v půdním roztoku nepříznivě ovlivňují schopnost půdních mikroorganismů rozkládat organickou hmotu i polutanty. Tato inhibice je důsledkem zúžení škály bakterií v zemině.
Mobilita sloučenin ve vodném prostředí závisí na jejich rozpustnosti. Zatímco oxidy a sulfidy kadmia jsou poměrně nerozpustné, chloridy a sírany rozpustné jsou. Koncentrace kadmia v sedimentech dna je obvykle více než desetkrát vyšší než ve vodě. Adsorpce kadmia na půdy a oxidy křemíku a hliníku silně závisí na hodnotě pH a vzrůstá s rostoucí alkalitou prostředí. Pokud je pH nižší než 6-7, dochází k desorpci kadmia z těchto materiálů. Zvýšením kyselosti (způsobené např. kyselými dešti) může dojít k uvolnění kadmia ze sedimentů a k výraznému zvýšení jeho koncentrace ve vodě. Kadmium je značně toxické pro vodní organismy, nejcitlivěji reagují lososovité ryby. Zvýrazňuje také toxicitu dalších kovů (zinku, mědi aj.) a negativně ovlivňuje samočisticí schopnost vody.
Dopady na zdraví člověka, rizika
Nejnebezpečnější sloučeniny Cd jsou CdO (NPK – 0,1 mg/m3 pro inhalaci), dusičnan kademnatý Cd(NO3)2 a síran kademnatý CdSO4. Kadmium je velmi toxický prvek, zvláště u zárodečných buněk, často je příčinou neplodnosti (teratogenní účinky). Způsobuje inhibici sulfhydroxylových enzymů (vazbou na SH-skupinu) a tím způsobuje kompetici s Fe, Zn a Cu v těle (vytěsňuje je). Otrava inhalací par při tavení, sváření Cd slitin je spojena s účinkem CdO (tzv. horečka slévačů), může způsobit rozedmu plic (CHOPN) ale i zvětšení pravé srdeční komory. Cd se váže v játrech na metaloproteiny (nízkomolekulární protein obsahující cystein-jedna ze stavebních aminokyselin proteinů), dále zasahuje do metabolismu sacharidů a inhibuje sekreci inzulínu. Akutní otrava se projevuje sliněním, zvracením, průjmy, závratěmi, bezvědomím až smrtí (latentní perioda je cca 24 hodin). Chronické otravy mají nespecifický průběh – zlatožlutý lem u zubů, hubnutí, žlutá barva kůže, kašel, dušnost, bolesti na prsou, celkové vyčerpání i smrt. Pro člověka je denní dávka z potravy (zelenina, konzervy, voda) 10 – 60 µg. Z toxikologicky nejvýznamnějších organických sloučenin Cd lze uvézt dimethylkadmium (CH3)2Cd a diethylkadmium (C2H5)2Cd, které se vlivem tepla a vzdušného kyslíku nebo vlhkosti rozkládají na CdO (často za exploze). Jsou považovány za suspektní karcinogeny (prostata, plíce).
Kadmium má velmi vysoký akumulační koeficient, detoxikace je proto pomalá a hrozí nebezpečí chronických otrav. Uvádí se, že má poločas vylučování přibližně 10 let a zároveň schopnost ukládat se v ledvinách, takže až 50 % kadmia uloženého v těle se nachází právě v ledvinách. Z tohoto důvodu řadíme Cd mezi nefrotoxické látky, protože způsobuje dysfunkci proximálních tubulů, záněty ledvin a nakonec i chronické selhávání ledvin. Vyšší obsah kadmia působí na metabolismus vápníku a způsobuje jeho zvýšené vylučování z organizmu s následkem zeslabení kostní hmoty. Podle klasifikace US EPA je Cd zařazen mezi lidské karcinogeny, může způsobovat rakovinu plic, ledvin a prostaty (vytěsňováním Zn z prostaty). Je teratogenní (poškozující plod). Z dalších účinků je významné poškození jater, kostí, plic a gastrointestinálního traktu. Chronické expozice mohou také způsobovat poškození srdce a imunitního systému. Kromě toho zesiluje toxické účinky jiných kovů, například zinku a mědi. Je jednoznačně prokázáno, že v náhodně vybraném vzorku populace obsahují ledviny silného kuřáka minimálně 10× více kadmia než u nekuřáka.
V České republice platí pro koncentrace kadmia a jeho sloučenin následující limity v ovzduší pracovišť: PEL – 0,05 mg.m-3, NPK - P – 0,1 mg.m-3.
Celkové zhodnocení nebezpečnosti z hlediska životního prostředí
Kadmium je velmi toxický prvek, který má schopnost hromadit se v potravních řetězcích. Může se vyskytovat ve všech složkách životního prostředí a akumulovat se v půdách a sedimentech s rizikem potenciálního nárazového uvolnění například změnou pH. Jeho toxické působení na člověka je skutečně mimořádně závažné. Zcela důvodné je proto pečlivé sledování emisí a jejich minimalizace.
Způsoby zjišťování a měření
Odhad emisí kadmia je možné provést pomocí bilance kadmia, tedy pomocí rozdílu množství kadmia v surovině a v produktu. Pokud je nutné znát přesné množství emitovaného kadmia, je nutné přistoupit k analýze jeho koncentrace v odcházejícím materiálu (vzdušnina, voda, kaly atd.).
Pro stanovení kadmia v atmosférickém aerosolu se používá odběr aerosolu na filtr s následnou mineralizací kyselinou dusičnou. Analýza mineralizátu se nejběžněji provádí pomocí atomové absorpční spektrometrie (AAS). Používá se atomizace v plamenu nebo elektrotermicky.
Pro stanovení Cd ve vodných roztocích lze obecně použít techniku atomové absorpční spektrometrie (AAS), dále techniku ICP-AES (emisní spektrometrie s indukčně vázaným plazmatem) nebo ICP-MS (hmotnostní spektrometrie s indukčně vázaným plazmatem). Pro stanovení Cd ve specifických matricích je k dispozici řada normovaných postupů:
| Norma | Metody měření Cd | Oblast použití |
| EN 14385:2004* | Stanovení celkových emisí As, Cd, Cr, Co, Cu, Mn, Ni, Pb, Sb, TI a V | Kvalita ovzduší, emise ze stacionárních zdrojů |
| EN ISO 11885:2009 | Stanovení 33 prvků atomovou emisní spektrometrií s indukčně vázaným plazmatem (ICP AES) | Kvalita vod |
| EN ISO 5961:1995 | Stanovení Cd metodou AAS | Kvalita vod |
* Evropská norma EN 14385:2004 má status české technické normy.
Vzorky půdy či kalů se před vlastním stanovením kadmia mineralizují kyselinou dusičnou. Při analýze vodných vzorků odpadá nutnost mineralizace. Kadmium se stanovuje pomocí atomové absorpční spektrometrie. Služby nabízejí komerční laboratoře.
Ohlašovací práh do vod 5 kg za rok si lze například představit jako objem vypuštěné vody 500 m3 o koncentraci kadmia 10 mg.l-1. V případě kadmia ve vzduchu o koncentraci 100 mg.m3 představuje ohlašovací práh 10 kg ročně objem vzduchu 100 000 m3 (za stejné teploty a tlaku jako je uvedena koncentrace).
Další informace, zajímavosti
Kadmium díky svým toxickým účinkům na životní prostředí i člověka, podléhá autorizaci REACH. S 34% podílem na globální produkci Cd byla Čína např. v roce 2013 největším producentem Cd na světě (7400 tun). Cd bylo poprvé objeveno v roce 1817 jako nečistota v minerálu Smithsonitu. Nejznámějším případem otravy kadmiem byla tzv. nemoc itai-itai. Japonská těžební společnost Mitsui Mining and Smelting Co., Ltd vypouštěla v letech 1910 až 1945 do řeky odpadní vody s obsahem kadmia. Tyto vody sloužily k zavlažování rýžových polí a k rybolovu. Vzhledem k vysokému bioakumulačnímu koeficientu kadmia docházelo k vysoké akumulaci kadmia v rýži a rybách a následně k otravám lidí. U lidí docházelo k ukládání kadmia v kostech, kde nahrazovalo vápník a tím způsobovalo křehnutí kostí. U kostí s uloženým kadmiem se zvyšuje nebezpečí zlomenin, lidé trpí bolestmi kloubů a zad (itai-itai znamená bolí-bolí).
Obrázek 1 ukazuje vztahy mezi koncentrací kadmia a možným ohrožením. Graf je k dispozici na webových stránkách agentury US EPA (USA).
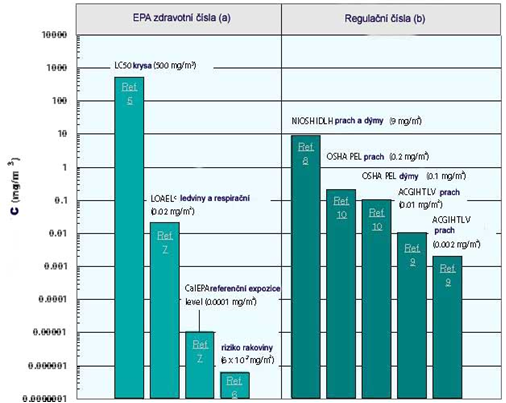
Obrázek 1: Vztahy mezi koncentrací kadmia a možným zdravotním rizikem
Informační zdroje
- Encyklopedie Wikipedia, https://cs.wikipedia.org/wiki/Kadmium, https://en.wikipedia.org/wiki/Cadmium
- Agency for Toxic Substances and Disease Registry, https://www.atsdr.cdc.gov
- Environment Agency, https://www.gov.uk/government/organisations/environment-agency
- PubChem, Open Chemistry Database, https://pubchem.ncbi.nlm.nih.gov/compound/23973
- Centers for Disease Control and Prevention, https://www.cdc.gov/niosh/topics/cadmium/
- US EPA IRIS, https://cfpub.epa.gov/ncea/iris2/chemicalLanding.cfm?substance_nmbr=141
- Pitter P.: Hydrochemie, Vydavatelství VŠCHT, 1999
- Horáková M.: Analytika vody, VŠCHT Praha, 2003
- Harte J., Holdren C., Schneider R., Shirley Ch.: Toxics A to Z, A Guide to Everyday Pollution Hazards, University of California Press, 1991
- Weiner E. R.: Applications of Environmental Chemistry, A Practical Guide for Environmental Professionals, Lewis Publishers, 2000
- Statistická ročenka životního prostředí České republiky, ČSÚ, 2003
- Státní zdravotní ústav, http://www.szu.cz/
- Igor Linhart: Toxikologie, VŠCHT Praha, 2014
- Paleček J., Linhart I., Horák J.: Toxikologie a bezpečnost práce v chemii, VŠCHT Praha 2004
- European Industrial Emissions Portal, https://industry.eea.europa.eu/pollutants/pollutant-index
- ČSN online, https://csnonline.agentura-cas.cz/
- Right to Know Hazardous Substance Fact Sheets, State of New Jersey Department of Health, https://web.doh.state.nj.us/rtkhsfs/indexfs.aspx